Интеграция и инновации разлагаемых полиэфирных материалов и технологий 3D-печати
Разлагаемые полиэфирные материалы:Разлагаемые полиэфирные материалы представляют собой класс биоразлагаемых полимерных материалов, которые могут постепенно разлагаться на небольшие молекулы в естественной среде или посредством ферментативного гидролиза организмов, и в конечном итоге поглощаться организмами или выводиться из организма. Этот вид материала имеет широкие перспективы применения в медицинской сфере из-за его хорошей биосовместимости, разлагаемости и производительности обработки.
Распространенные разлагаемые полиэфирные материалы:включая полимолочную кислоту (НОАК), полигликолевую кислоту (ПГА), полиε-капролактон (ПКЛ), политриметилкарбонат (ПТМК), полип-дициклогексанон (ППДО) и так далее. Цикл деградации, механические свойства и гидрофильность этих материалов можно контролировать с помощью различных соотношений мономеров и методов сополимеризации для удовлетворения различных медицинских потребностей. Разлагаемые полиэфирные материалы в сочетании с технологией 3D-печати демонстрируют большой потенциал в персонализированной медицинской настройке, могут точно изготавливать сложные медицинские имплантаты, которые отвечают потребностям пациентов, хирургические направляющие и т. д., для достижения точной медицины в то же время, материал может быть усвоен организмом после завершения задачи, снизить риск вторичной хирургии и способствовать реабилитации пациентов.
Во-первых, индивидуальная разработка разлагаемых полиэфирных материалов для медицинских целей.
Индивидуальная реализация
1. Соотношение мономеров и метод сополимеризации:
Регулируя соотношение мономеров и режим сополимеризации разлагаемых полиэфирных материалов, можно точно регулировать период разложения, механические свойства и гидрофильность разлагаемых полиэфирных материалов. Например, сополимер ПЛКЛ полимолочной кислоты (НОАК) и polε-капролактона (ПКЛ) может контролировать скорость разложения и механические свойства материала, изменяя соотношение НОАК и ПКЛ.
2. Проектирование структуры молекулярной цепи:
Молекулярная структура цепи полимера, такая как размер молекулярной массы и ширина распределения, модификация концов, блок, разветвление, сшивание, гиперразветвленность и т. д., может дополнительно контролировать свойства материалов. Например, прочность и ударная вязкость полимолочной кислоты могут быть улучшены путем введения пластичных сегментов цепи или построения сшитых сетей.
3. Контроль структуры агрегации:
Контролируя структуру агрегации полимеров, такую как ориентация и кристаллизация, можно контролировать цикл деградации и механические свойства материалов. Например, механическое самоусиление может быть достигнуто путем индуцирования ПЛЛА для образования волокнистых кристаллов посредством черновой ориентации. Цикл деградации материалов ПЛЛА можно контролировать, регулируя кристалличность материалов ПЛЛА с помощью зародышеобразователей.
4. Смешивание дизайна:
Текстурная структура гетерогенной системы может быть разработана путем смешивания и других средств для эффективного управления эксплуатационными характеристиками разлагаемых полиэфирных материалов. Например, механическая прочность и биологическая активность разлагаемых полиэфирных композитов могут быть улучшены путем смешивания биоактивных неорганических наноматериалов. Смешивая проявляемый материал, проявляемому полиэфирному материалу может быть придан проявляемый эффект.
Примеры персонализированных приложений
1. Тканевая инженерия и регенеративная медицина:
Разлагаемые полиэфирные материалы могут использоваться для изготовления 3D-печатных стентов для тканевой инженерии, которые могут быть персонализированы в соответствии с конкретными потребностями пациентов. Например, регулируя скорость деградации и механические свойства материала, можно подготовить каркас, соответствующий тканям пациента, тем самым способствуя регенерации и восстановлению тканей.
2. Хирургические средства:
Технология 3D-печати также позволяет изготавливать хирургические приспособления, такие как хирургические направляющие, хирургические модели и т. д. Эти инструменты могут помочь врачам моделировать и планировать операции перед операцией, повышая точность и безопасность хирургического вмешательства.
3. Биоразлагаемые медицинские изделия:
Такие устройства, как биоразлагаемые стенты, могут постепенно разрушаться после имплантации в организм, избегая долгосрочных рисков, которые могут быть вызваны традиционными металлическими стентами. В то же время, индивидуальный дизайн биоразлагаемых стентов может лучше адаптироваться к сосудистой структуре пациента и улучшить эффект лечения.
ПКЛ, НОАК и ПЛКЛ имеют свои собственные характеристики в области биомедицинских материалов. ПКЛ обладает хорошей биосовместимостью, контролируемой деградацией и превосходными механическими свойствами. Однако скорость деградации медленная, а прочность относительно низкая. НОАК обладает полной биодеградацией, хорошими технологическими характеристиками и высокой механической прочностью. Но хрупкость велика, скорость деградации может быть слишком быстрой.
ПЛКЛ сочетает в себе прочность ПКЛ с прочностью НОАК, имеет контролируемый цикл деградации, превосходные механические свойства и хорошую биосовместимость. Подходит для различных применений в тканевой инженерии, таких как восстановление хрящей, нервных проводников, сосудистых стентов и костей. Применение технологии аддитивного производства ПЛКЛ в тканевой инженерии имеет значительные преимущества и потенциал.
Во-вторых, применение технологии аддитивного производства ПЛКЛ в тканевой инженерии
1. Наружный трахеальный стент:
Материал ПЛКЛ с функцией памяти формы используется для изготовления внешнего трахеального стента с персонализированной формой и размером с помощью технологии 3D-печати. Стент может быстро возвращаться к заданной форме после имплантации, обеспечивать стабильную поддержку трахеи и иметь хорошую биосовместимость и способность к деградации.

2. Грудные имплантаты:
Персонализированные грудные имплантаты изготавливаются с использованием разлагаемых полиэфирных материалов в соответствии с требованиями к форме и размеру груди пациента. Имплантат способен постепенно разлагаться с течением времени и в конечном итоге рассасываться организмом, избегая долгосрочных осложнений, которые могут возникнуть при использовании традиционных имплантатов.

3. Другие медицинские приборы:
Разлагаемые полиэфирные материалы также могут использоваться для изготовления персонализированных ортопедических имплантатов, сердечно-сосудистых интервенционных устройств, рассасывающихся швов и других медицинских устройств. Эти устройства могут быть адаптированы к индивидуальным потребностям пациентов, что улучшает результаты лечения и качество жизни пациентов.
Полимерный материал успешно применил технологию аддитивного производства ПЛКЛ в тканевой инженерии и распространил свое применение во многих областях, таких как медицинская 3D-печать проволоки, биологическая 3D-печать и СЛС 3D-печать сырья для медицинских микросфер.
В-третьих, применение разлагаемых биомедицинских материалов.
Медицинская проволока для 3D-печати
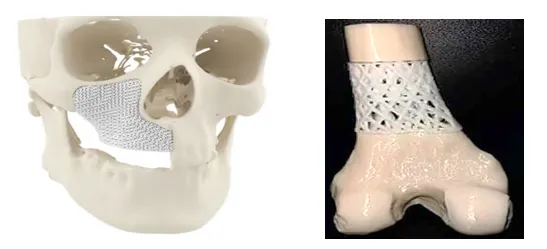
Медицинская проволока НОАК имеет важное прикладное значение в 3D-печати челюстно-лицевой кости/черепного восстановления, пористых каркасов для восстановления хряща, сосудистых каркасов и т. д. Ее хорошая биоабсорбируемость, высокая прочность и пластичность, а также хорошая биосовместимость делают линии НОАК 3D-печати широко используемыми в медицинской сфере. Примерами являются рассасывающиеся имплантаты челюстно-лицевой кости и пористые каркасы для восстановления кости.
Применение медицинских микросфер в СЛС 3D-печати
23 июля 2024 года технология под названием дддхххА Медицинский 3D печать контролируемый микросфера подготовка обработано", успешно разработанная Шэньчжэнь Гуанхуа Вейе Ко., ООО. и ее дочерней компанией Шэньчжэнь Цзюшэн Биотехнология Ко., ООО., официально прошла проверку Государственного ведомства интеллектуальной собственности и получила национальное патентное разрешение на изобретение. Изобретение направлено на разработку процесса подготовки, который гарантирует, что микросферы, используемые в медицинской 3D-печати, имеют контролируемый размер частиц и скорость биодеградации.
Суть процесса подготовки заключается в достижении точного контроля размера частиц и скорости биодеградации микросфер, что обеспечивает надежную поддержку применения технологии СЛС 3D-печати в медицинской сфере.
1. Система доставки лекарств:
Медицинские микросферы могут использоваться в качестве носителей для систем доставки лекарств, а микросферы с определенными структурами и свойствами могут быть точно изготовлены с помощью технологии СЛС 3D-печати. Эти микросферы могут переносить ингредиенты лекарств и достигать точного высвобождения лекарств в организме, повышая эффективность лекарств и уменьшая побочные эффекты.
2. Каркасы для тканевой инженерии:
Технология 3D-печати СЛС может использоваться для подготовки каркасов для тканевой инженерии с бионической структурой и механическими свойствами. Медицинские микросферы, входящие в состав каркасов, могут обеспечивать поддержку и питание, необходимые для роста клеток, а также способствовать регенерации и восстановлению тканей.
3. Микросреда для клеточной культуры: с помощью технологии СЛС 3D-печати можно подготовить микросреду для клеточной культуры с микропористой структурой и сложной геометрией. Как часть микросреды, медицинские микросферы могут обеспечить точки прикрепления и питательные вещества, необходимые для роста клеток, а также оптимизировать условия для клеточной культуры.
3D-биопечать
ПКЛ — это термопластичный полиэфир с хорошей биосовместимостью, разлагаемостью и механическими свойствами. Сырье ПКЛ может обрабатываться различными технологиями 3D-печати (такими как моделирование методом послойного наплавления FDM, селективное лазерное спекание СЛС и т. д.) для формирования 3D-печатных изделий со сложными структурами и функциями.
Экструзия расплава частиц является важным процессом в биопечати, который включает нагревание частиц ПКЛ до расплавленного состояния и последующую их экструзию через сопло на печатную платформу для формирования 3D-структур слой за слоем. Этот процесс имеет преимущества высокой точности, высокой эффективности и высокой гибкости для удовлетворения различных медицинских потребностей.
1.Тканевая инженерия:
ПКЛ может использоваться в качестве материала для тканевой инженерии, чтобы поддерживать рост и дифференциацию клеток, а также способствовать восстановлению и регенерации тканей. С помощью технологии биопечати можно подготовить тканевые инженерные каркасы со сложными структурами и функциями, чтобы обеспечить лучшую поддержку для восстановления и регенерации тканей.
2. Хирургическое планирование:
Сырье ПКЛ используется для печати 3D-моделей определенных частей тела пациентов, что помогает хирургам проводить хирургическое планирование и имитационные операции. Это может повысить точность и безопасность хирургических вмешательств, а также снизить хирургические риски.
3. Медицинские приборы и имплантаты:
Сырье ПКЛ также может использоваться для изготовления медицинских устройств и имплантатов, таких как хирургические направляющие, костные штифты, костные пластины и т. д. Эти медицинские устройства и имплантаты обладают хорошей биосовместимостью и механическими свойствами и могут соответствовать различным медицинским потребностям.




